| 원소 분류 (배경색) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 알칼리 금속 | 알칼리 토금속 | 란타넘족 | 악티늄족 | 전이 금속 | 전이후 금속 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 준금속 | 비금속 | 할로젠 | 비활성 기체 | 미분류 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 상온(298K(25°C), 1기압 )원소 상태 (글자색) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ● 고체 | ● 액체 | ● 기체 | ● 미분류 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 이탤릭체 : 자연계에 없는 인공원소 또는 극미량으로 존재하는 원소 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
{{틀:주기율표/설명문서}}
週期表
Periodic Table
1 개요
원소주기표[1]는 자연계에 존재하는, 그리고 인공적으로 만들어 낸 모든 원소를 그 원자번호와 원소의 화학적 특성에 따라 나열한 표이다. 기초적인 지식이 있다면 물질의 화학적 성질을 쉽게 예측할 수 있게 하며, 100개가 넘는 원소의 특징을 체계화한 데 큰 의미가 있는 물건이다.
기본적인 주기표는 위의 형태에 더해 원자번호, 원자량, 원소의 화학적 특성에 따른 분류(비금속[2], 금속[3], 준금속[4]), 주요 산화수, 간혹가다 전자배치 정도를 표시하고 있다 그러나 화학에 대한 지식이 있는 사람이면 원소의 위치(족[5],주기[6]등, )와 그 원자번호(양성자의 수=이온화 안 됐을 때의 전자의 수, 바닥상태의 전자배치 등)를 보고 원소에 대해 어느 정도의 정보를 얻을 수 있게 되어 있다.
위의 정보 외에도 용도에 따라 다양한 정보를 포함하는 주기표 역시 존재한다.
주기표의 형태는 보통(이 아니고 거의) 위와 같은 직사각형 표와 같은 형태지만[7] 직사각형 형태가 아닌 형태의 주기율표도 많이 있긴 하다. 대개 입체라서 만들기 힘들어서(...) 잘 안쓰며, 보통은 보기조차 힘들지만. 주기율표 자체를 교과서나 연구실 이외에서 보기 힘드니...
한편으로는, 거의 알려지지 않았지만 문화적으로 뭔가 임팩트를 남겼는지 원소가 아닌 다른 것들의 주기표 같은 것도 존재한다. 그 분야의 덕후들이 덕질을 위해선지 그렇게 변형해 쓰고 있다.
주기표의 다양한 형태와 각기 어떤 정보를 담고 있는지 보고 싶다면 구글 이미지 검색에서 periodic table로 검색해보자. 형태를 보면 대부분 맨 위에 보인 직사각형 형태지만 그렇지 않은 것도 상당히 많다. 별난 형태의 주기표만 찾아보고 싶다면 alternative periodic tables으로 검색해보자그 수도 상당해서 2015년 2월 기준 대략 3백7십만개 이상 나온다. 물론 겹치는 것도 있을 것이고, 보여주는 것 자체가 앞의 1000개 뿐이지만... 어쨌든 엄청나게 많다. 네이버캐스트에서도 주기표 순서로 원소의 특성을 연재중이다. 보러 가기 2010년 7월 26일부터 1~2주에 한 번씩 연재해 왔으며, 2014년 3월 12일부로 현재까지 발견된 마지막 원소인 오가네손(당시 명칭 우누녹튬)까지의 연재를 완료하였다.
아직 발견되지 않은 119번 이후의 원소 위치를 예상하여 만든 확장 주기율표가 있다. 무식하게 7주기 이전과 같은 방식으로 만든 주기율표는 잘못된 주기율표이고, Fricke가 만든 주기율표(52칸짜리, 32칸짜리)과 2011년에 페카 퓌쾨(Pekka Pyykkö)라는 핀란드 화학자가 제안한 퓌쾨 모델(Pyykkö Model)이라는 주기율표가 있다. 퓌쾨 모델은 138번까지는 위의 확장 주기표와 같으나 운트리엔늄(원소 139번)과 운쿼드닐륨(원소 140번)이 생뚱맞게 오른쪽으로 갔다가 운쿼드우늄(원소 141번)부터 다시 왼쪽으로 가는 등 원소 위치가 더 복잡하다. 그 이유는 8주기 원소 항목에도 언급되었듯이 5g부터 8p 오비탈까지 에너지가 비슷해서 채워지는 순서가 제멋대로일 것으로 예측되기 때문이다. 자세한 것은 영문 위키백과의 문서 참고. 현재 영문 위키백과에서와 한국어 위키백과에서는 119번 이후의 원소 문서에서 Fricke식의 주기표를 사용한다. 나무위키의 틀:확장 주기율표도 마찬가지.
참고로 주기표에는 J/j와 Q/q가 쓰이지 않는다. q의 경우 플레로븀이 우눈쿼듐(Uuq)이었을 때 잠깐 쓰이긴 했지만...만약 운비쿼듐이 발견되면 다시 쓰일 수도 있다. J는 쓰일 뻔했으나 113번 원소를 자포늄이 아닌 니호늄으로 이름붙이면서 쓰이지 않게 되었다.
1.1 주기율표/중국어
중국어판은 주기율표/중국어 문서 참고. 화학 천자문 같다 한자로 주기율표를 만들었다.
2 역사
드미트리 멘델레예프가 최초의 주기표를 고안해 냈으며[8], 그 역사는 초기 화학의 역사 그 자체라고 할 수 있을 정도이다. 화학 교육도 이론적인 부분을 여기서 시작한다.
존 돌턴의 원자설이 등장한 이후 근대 화학은 맹렬하게 발전하기 시작했는데, 그 발전 과정에서 다양한 원소들이 발견되었다. 이 원소들은 특정한 성질을 공유하는 그룹으로 묶일 수 있었고, 따라서 원소들이 보이는 주기성에 관한 다양한 해석들이 나왔다.
그렇지만 이런 주기성에 대한 해석들은 전부가 주류가 될 만큼 인정받지 못했다. 어찌보면 당연한 것이, 당시에는 아직 발견하지 못한 원소도 있었고 원소인 것으로 알려졌지만 실제로는 아닌 것도 있었으며, 또한 이런 특성과 주기성을 연결하기 위한 현재의 원자번호에 해당하는 개념이 정착되지 않았다. 따라서 이론들은 그야말로 엉성하기 그지없었다. 당연히 이런 이론들은 나오기 무섭게 무차별로 공격당하고는 사라졌다.
이 쪽으로는 뉼랜즈의 옥타브설이 유명한데, 화학Ⅰ 2단원 중에 옥타브설이 소개되어 있는 부분이 있으니 그 곳을 참고하면 2주기까지는 그럭저럭 맞아떨어지다가 3주기에 들어가서는 주기성이 사정없이 깨지는 것을 알 수 있다. 그런 문제도 있고, 당시 화학계에서 뉼랜즈는 이 가설을 발표하고 나서 화학 원소 가지고 음악이라도 연주하는 거냐? 알파벳 순서로도 한번 배열해보지?라는 비판을 들었는데, 이 때문에 삐쳐서 과학을 포기하게 되었다고 한다. 하지만 나중에 멘델레예프의 주기표가 인정을 받고 난 뒤 (1872년, 22년 뒤) 영국 화학회에선 뉼랜즈의 시도도 의미가 있었다고 하며 나중에 불러 상을 주었다고 하니 인간만사 새옹지마.
어쨌든 이런저런 각종 잡설(...)이 난무하던 화학계에 빛을 던진 것이 바로 멘델레예프. 그는 이 주기표를 원소들이 적힌 플레잉 카드로 카드 게임을 하다가 생각해냈다고 하며[9], 원자량과 화학적 성질을 통해 현 주기율표의 원초적인 형태를 고안해냈다. 이 원초적인 형태는 주기표의 1~3주기에선 현재도 거의 그대로 사용되고 있다. 소위 단주기 주기표라고 부르는 그것.
멘델레예프는 위에서 전술한 장애물을 오히려 반대로 이용하였다. 주기성을 훼손시키는 원소에 대해서 발견되지 않은 원소가 사이에 있음을 가정하고 자리를 비워놓은 후 주기성에 입각해서 물리화학적 특성을 예언하였고[10], 원소로 잘못 인지되었던 화합물에 대해선 과감하게 빼버렸으며[11], 다른 사람이 발견한 원소의 특성에 대한 보고서의 잘못된 부분을 보고 주기성을 감안하면 잘못된 결과이니 다시 실험해서 수정하라는 조언까지 하기도 하였다[12]. 물론 멘델레예프와 그의 이론이 신은 아니었으므로 그가 말한 이런저런 예언이나 설명이 전부 맞아떨어진 것은 아니다. 다만 아래 표처럼 맞힌 게 정말 기가 막힐 정도로 정확했기 때문에 덮였다(...).
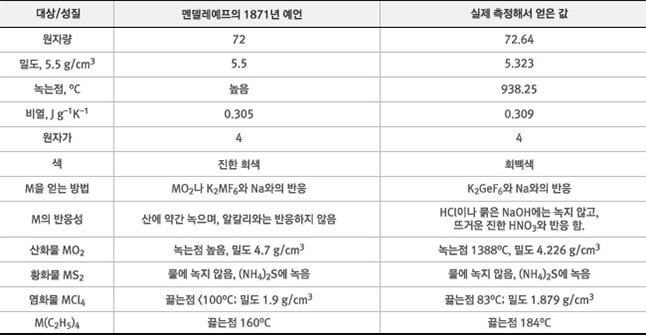 멘델레예프가 예측한 에카-규소와 실제 저마늄(게르마늄)의 특성 비교. 출처 |
위 표와 같이 존재조차도 모르던 원소의 물리량이나 화학적 특성을 작두탄 수준으로 맞췄으니 주목을 받지 않을래야 않을 수가 없다. 이 사례는 대한민국 화학II 교과서에도 단골로 나올 정도며, 에카규소 이외에도 에카붕소(스칸듐), 에카알루미늄(갈륨), 에카망간(테크네튬) 등을 기가막히게 맞춰냈다.
이후 헨리 귄 제프리스 모즐리라는 비운의 천재가 이전의 원자질량 구분법으로 인한 화학성질과 원자량의 불일치[13]를 X선으로 원자번호를 결정하는 방식(=핵의 양성자 수)으로 해결해내면서 현재의 주기표가 만들어질 수 있게 되었다.
훗날 멘델레예프는 사후 이 엄청난 공적을 인정받아 101번 원소의 이름이 그의 이름을 따서 지어지게 된다. 참고로 불안정한 게 그의 말년 성격과 닮았다고 한다.
3 외워야 하나?
화학을 배우지 않은 사람들이 이걸 처음 접하면 '이걸 다 외워야됨?'이라며 깜짝 놀라곤 하는데, 외울 필요 없다고는 하지만 사실 어느 정도는 외워야 한다. 고등학교 과정에서도 20번까지만 외우면 만사 오케이. 초등학생이 80번인 수은까지 외우고 다니는 경우도 봤다
-수헬리베붕탄질산플레나마알규인황염아칼칼![14][15] 사실 유럽이나 미국의 학교에서는 항상 주기표를 제공한다. 대학에 가도 교실 한쪽 벽에는 항상 큰 주기표가 걸려있어서 그거 힐끔힐끔 보면서 수업한다.[16] 무기화학 교수님이 전이원소까지 다 외우라고 하더라 시험 칠 때 앞에 있던 주기율표 뗐다 어지간한 학부 수준 화학책 맨 앞에 붙어있기도 하고... 게다가 대학에서 필요한 건 원소 번호 몇 번 이런 게 아니라 원자량이나 전자 친화도같이 원소들의 물리적 화학적 특성값이라서 어차피 찾아봐야 한다. 가끔씩 이걸 다 외우는 사람이 있긴 한데, 그건 필요해서 그러는 게 아니다. 어쩌다 보니 외워졌거나 순수한 취미다. 취향이니 존중해주자. 다만 주기율표의 원소가 워낙 많기 때문에, 주기율표를 외우고 있는 사람과 그렇지 않은 사람의 주기율표 해독 속도는 큰 차이가 난다. 시험을 볼 때 주기율표를 주기는 하지만, 주기율표를 외우고 있지 않다면 시간을 낭비하게 될 가능성이 높다는 뜻. 시험시간이 부족하게 느껴진다면 주기율표를 외워보자.
중고생이라면 칼슘까지는 번호순을 외우는 게 좋다. 약간 머리를 굴려주면 암기사항의 일부는 원자번호나 원자량에서 유도되기 때문. 하지만 원소 이름부터 수소나 산소 등 몇몇을 제외하고는 대부분 외래어 인데다가 첫 음절에 '베', '헬', '플' 등 우리말에서 잘 사용되지 않는 음절들이 많이 나오기 때문에 적절히 만들만한 문장도 없기 때문에 외우는 방법이 그렇게 녹록치 않다. 이걸 이용해 끝말잇기를 한다면...
교사나 강사들은 지구과학 영역에서의 '활 잘 쏘는 석방형이 인정 없는 석황을 강금했다.'[17]나 'Oh! Be a fine girl kiss me.'[18]풀(플루오린)뜯어먹는 염소 불X(브로민)이(아이오딘)처럼 그럴듯한 암기법을 개발해 보려고 하고, 흔히 알고 있는 노래에 붙여보기도 하고, 다들 한 가지씩의 암기법을 가지고 있고 그것대로 외우도록 가르치지만 사실 뭐라고 외워도 어색하다.
4 외워보자
항목이 길어지고 쓸데없는 것 같아 분리하였다.원소 외우기 문서 참조.
5 관련 작품이자 동명의 산문집
화학자/문필가인 프리모 레비가 저술한 산문집. 유태인인 레비가 수용소 생활이나 자신의 생각 등을 담았다. 원소 이름이 각 챕터의 이름인데, 상당히 훌륭한 내용이다.
6 화학어
백괴사전에 나오는 내용이며 인터넷에도 떠돌아다니는 일종의 언어로 영어 단어(또는 문장)의 알파벳을 모조리 다 주기율표의 원소기호로 바꿔 이야기하는미친 언어이다. 대표적인 예로 규소붕소알루미늄이 있는데 이를 주기율표로 변환하면 Si B Al이다. 한번 붙여서 읽어보자. 또 플루오린우라늄탄소칼륨도 있다. fxxx 화학에 약한 사람들에게 욕을 하고 싶을 때 사용하면 좋다. 고등학교 올라갈 땐 제발 이런 건 떼고 올라가자 100Zn은 이 사람이라 카더라
- ↑ 사실 주기율표는 잘못된 말이다. 주기율은 화학적 성질이 비슷한 원소가 일정한 간격을 두고 주기적으로 나타내는 성질을 말하는데 이 표는 이것을 나타내기 위한 것이 아니라 원소의 주기 그 자체를 나타내기 위한 것이기 때문이다. 즉 주기표 또는 원소주기표가 옳은 말이다. 이 사실은 이 표의 영어 표기를 보면 쉽게 알 수 있다.영어로도 Periodic table이지 Periodic law table이 아니다. 다만 나무위키에서는 대한민국에서는 주기율표라는 말이 통용되고 있음을 고려하여(심지어 이를 올바르게 교정해야 할 대한화학회조차도 '주기율표'를 사용하고 있는 실정이다.) 표제어는 주기율표를 사용한다.
- ↑ 전자를 받아서 비활성 기체와 같은 최외곽 전자배치를 가지려는 성질을 지는 원소들
- ↑ 전자를 잃어서 비활성 기체와 같은 최외곽 전자배치를 가지려는 성질을 지니는 원소들
- ↑ 금속과 비금속의 중간격인 원소들로, 금속보다는 전자를 얻으려는 성질이 강하고, 비금속보다는 전자를 잃으려는 성질이 강한 원소들
- ↑ 왼쪽부터 오른쪽으로 갈수록 s-p(2주기부터)-d(4주기부터)-f(6주기부터)궤도순으로 전자가 채워지는데, 여기서 최외곽 전자배치가 똑같거나 거의 비슷한 녀석들끼리 화학적 성질이 비슷한 놈들을 세로줄(예: O,S,Se,Te,Po,Lv)로 나열한것이다
- ↑ "주양자수"라는것을 나타내며, 간단히 말하자면 전자를 채워넣을수 있는 오비탈의 에너지 준위와 종류(=전자 껍질의 수)를 나타낸다. 예를 들면 1주기는 전자를 넣을수 있는 오비탈의 종류가 단 1개(1s)이고, 3주기는 전자를 넣을수 있는 오비탈의 종류가 3종류(3s,3p,3d)이다(사실, 3주기에서는 원래 3s,3p만 집어넣는 경우가 많지만, 3d에 최외곽 전자를 집어넣는 경우도 간혹 보인다-DNA뼈대에서의 인산결합이 그 예
- ↑ 다만 위의 주기율표에서는 수소의 위치가 1족으로 되어 있지만 그 이중적인 화학적 특성 때문에 누가 만드느냐에 따라 1족 혹은 17족, 경우에 따라 두 곳 모두에 위치하는 경우도 있다. 또한 간혹 오비탈이 절반 비어있다는 이유로 탄소 위에 놓는 경우도 있다.
- ↑ 이 공로로 1906년 노벨 화학상을 수상할... 뻔했으나 1표 차이로 실패했다. 수상자는 플루오린의 분리에 성공한 무아상. 사실 플루오린은 그 무지막지한 반응성 때문에 순수한 형태로 분리하는게 지극히 어려우니, 무아상의 공로도 작은 건 아니다.
- ↑ 그래서인지 대부분의 화학2 교과서에선 주기표를 설명할 때 원소 카드를 갖고
그가 갖고놀던 방식으로 재현은 못하겠지만카드 놀이를 하는 활동을 꼭 시킨다.당연하지만 실제로 해 볼 리가 없다 - ↑ 아주 높은 정확도로 맞혔다!
- ↑ 역시 이후에 화합물로 밝혀졌다!
- ↑ 이것 역시 그대로 맞아떨어진다
- ↑ 주기표의 순서는 양성자 개수의 순서
- ↑ 단 30번까지 외우는 것을 더 추천한다. 30번 내로 주요 금속(티타늄, 철, 망가니즈, 아연, 코발트 등등)이 있기 때문에 화학을 좋아하는 학생들은 30번까지 외우고 다닌다.
- ↑ 단, 알칼리 금속, 알칼리 토금속, 할로젠 원소, 비활성 기체는 외우는 게 좋다
뭐가 이리 많아그냥 다 외우라는 거지? - ↑ 그러나 이것은 대학마다 다르다. 어떤 교수님은 전이 금속을 제외하고 모두 외워오라고 하기도 한다...
- ↑ 모스 경도계의 순서를 외우는 암기법
- ↑ 항성의 온도에 따른 색 스펙트럼 순서를 외우는 암기법으로 Oh! BoA fine girl kick me.
오! 보아, 예쁜 girl이 나를 차요오바마 fxcking gay kiss me등의 바리에이션도 있다. girl을 guy로 바꿔도 된다. - ↑ 이거 다 하면 엄청 복잡하다. 세상에서 제일 긴 영단어를 이걸로 변환해보자. 그러면 음...